La mole (simbolo: mol) dal 1971 è entrata a far parte delle sette unità fondamentali del Sistema Internazionale (SI).
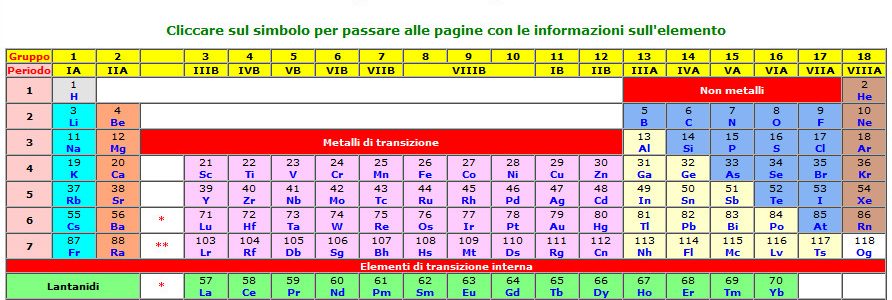
La mole è stata definita la quantità di materia che contiene un numero di particelle pari a quello degli atomi presenti in 12 grammi di Carbonio-12 (12C, l’isotopo del Carbonio più diffuso in natura).
Questo numero di particelle o insiemi delle stesse, quando espresso in mol-1, è detto numero o costante di Avogadro (NA), in ricordo dello scienziato italiano Amedeo Avogadro, ed è un numero molto grande:
NA = 6,02214076 ·1023 mol -1
da cui
1 mol = 6,02214076 ·1023 / NA
Una mole (1 mol) contiene 6,02214076·1023particelle (atomi, molecole, elettroni, protoni, neutroni e insiemi degli stessi).
Ad esempio, una mole di O2 (Ossigeno) contiene 6,02214076·1023 molecole; una mole di Fe (Ferro) contiene 6,02214076·1023 atomi di ferro.
Con questa definizione il valore della massa molare del Carbonio-12, M(12C), era pari a 0,012 kg/mol (12 grammi); ciò poteva ingenerare errori qualora, con ricerche sempre più raffinate, la stessa fosse determinata anche con minime differenze.
In altre parole, così come fatto per altre unità di misura, quali la lunghezza e la massa, la bontà del campione non poteva più essere considerata assoluta in quanto allora ed ancor oggi, non è possibile verificare sperimentalmente il numero esatto di atomi presenti in 0,012 kg (12 g.) di 12C.
Per questo motivo, nel 2018 la Conférence générale des poids et mesures (CGPM) ha stabilito che dal 20 maggio 2019 le sette unità fondamentali del SI dovessero essere definite in relazione a sette costanti fisiche. Nel caso della mole, la costante è, appunto, il Numero o Costante di Avogadro
Il cambiamento del paradigma, nel caso della mole, è una nuova definizione del valore della massa molare del Carbonio-12, M(12C) che non è più noto ma si deve ricavare sperimentalmente.
Dal punto di vista pratico, invero, non cambia nulla a livello stechiometrico.
Per approfondire l’argomento e per conoscere come sia possibile definire sperimentalmente la mole, è interessante questa brochure del Consultative Committee for Amount of Substance – Metrology in Chemistry and Biology (CCQM): https://www.bipm.org/utils/en/pdf/si-mep/SI-App2-mole.pdf
Un’altra interessante brochure sulla nuova definizione elle unità fondamentali del SI è disponibile presso il sito dell’Istituto Nazionale di Ricerca Metrologica (INRiM): https://www.inrim.it/ricerca-sviluppo/le-unita-di-misura/la-ridefinizione-del-sistema-internazionale-delle-unita-di